Gjenopplivingen av romtemperatur-natrium-ion-batterier
På grunn av de rikelige natriumreservene (Na) i jordskorpen og de lignende fysisk-kjemiske egenskapene til natrium og litium, har natriumbasert elektrokjemisk energilagring betydelig løfte for storskala energilagring og nettutvikling. For eksempel har høytemperatur nullutslippsbatteriforskningsaktivitetsceller basert på Na/NiCl2-systemer og høytemperatur Na–S-celler, som er vellykkede kommersielle tilfeller av stasjonære og mobile applikasjoner, allerede demonstrert potensialet til natriumbaserte oppladbare batterier. Imidlertid forårsaker deres høye driftstemperatur på rundt 300 °C sikkerhetsproblemer og reduserer rundreiseeffektiviteten til natriumionbatterier (SIB). Romtemperatur (RT) SIB-er blir derfor ansett som den mest lovende alternative teknologien til LIB-er.
I løpet av batterihistorien de siste 200 årene ble forskning på SIB-er intenst utført side om side med LIB-utvikling. Den elektrokjemiske aktiviteten til TiS2 for litium og dens gjennomførbarhet for energilagring ble først fremsatt på 1970-tallet. Etter denne oppdagelsen ble evnen til Na-ioner til å settes inn i TiS+2 realisert på begynnelsen av 1980-tallet. Med oppdagelsen av grafitt som et rimelig anodemateriale med moderat kapasitet for LIB-er og unnlatelsen av å interkalere natriumioner, skjedde en rask LIB-utvikling på 1990-tallet, og erstattet veksten i natriumkjemi. Så, i 2000, forynget tilgjengeligheten for natriumlagring i hardt karbon (HC), som ville levere en energikapasitet som ligner på Li i grafitt, forskningsinteressen for SIB-er.
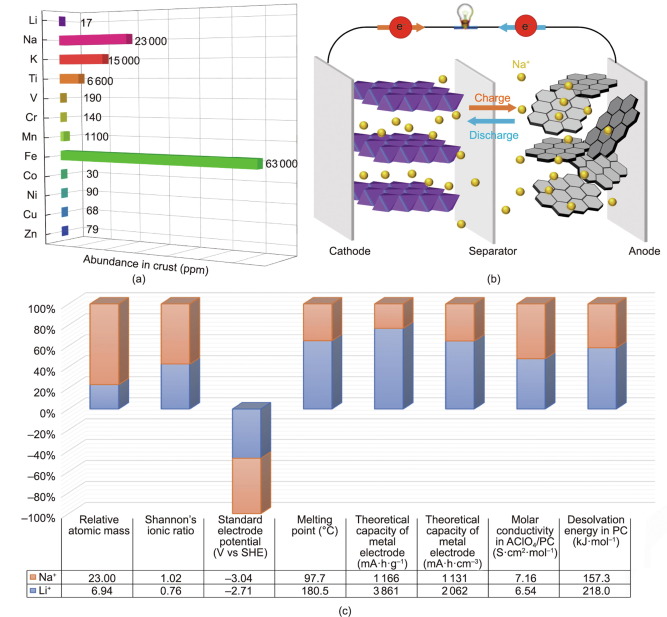
En sammenligning av natrium-ion-batteri og litium-ion-batteri
Gjenopplivingen av SIB-er – kombinert med det stadig økende presset fra mangelen på tilgjengelighet av litiumreserver og den tilsvarende eskaleringen i kostnadene – gir en komplementær strategi til LIB-er. SIB-er har fått økende forskningsoppmerksomhet, kombinert med grunnleggende prestasjoner innen materialvitenskap, i arbeidet med å tilfredsstille den økende penetrasjonen av fornybare energiteknologier. Cellekomponentene og de elektrokjemiske reaksjonsmekanismene til SIB-er er i utgangspunktet identiske med LIB-er, bortsett fra ladningsbæreren, som er Na i den ene og Li i den andre. Hovedårsaken til den raske ekspansjonen i SIB-materialkjemi tilskrives parallellene i fysisk-kjemiske egenskaper mellom de to alkalimetallene.
For det første er driftsprinsippene og cellekonstruksjonen til SIB-er lik de til kommersielle LIB-er, om enn med Na som ladningsbærer. Fire hovedkomponenter finnes i en typisk SIB: et katodemateriale (vanligvis en Na-holdig forbindelse); et anodemateriale (som ikke nødvendigvis inneholder Na); en elektrolytt (i flytende eller fast tilstand); og en separator. Under ladeprosessen ekstraheres natriumioner fra katodene, som typisk er lagdelte metalloksider og polyanioniske forbindelser, og blir deretter satt inn i anodene, mens strømmen går via en ekstern krets i motsatt retning. Ved utlading forlater Na anodene og går tilbake til katodene i en prosess som kalles "gyngestolprinsippet". Disse likhetene har muliggjort den foreløpige forståelsen av og rask vekst i SIB-teknologi.
Dessuten gir den større ioniske radiusen til Na sine egne fordeler: økt fleksibilitet av elektrokjemisk positivitet og redusert desolvatiseringsenergi i polare løsningsmidler. Det større gapet i den ioniske radiusen mellom Li og overgangsmetallionene fører vanligvis til svikt i fleksibiliteten til materialdesign. I motsetning til dette muliggjør et natriumbasert system mer fleksible faste strukturer enn et litiumbasert system, og har enorm ionisk ledningsevne. Et typisk eksempel er β-Al2O3, hvor Na-interkalering har perfekt størrelse og høy ledningsevne. Mer lagdelte overgangsmetalloksider med forskjellige M+x+ stablingsmåter kan enkelt realiseres i et natriumbasert system. Tilsvarende er det store utvalget av krystallstrukturer som er kjent for natriumioniske ledere (NaSICON) familien mye mer komplisert enn litiumanalogene. Enda viktigere, en mye høyere ionisk ledningsevne kan tillates i NaSICON-forbindelser, som langt overstiger ionisk ledningsevne i litiumioniske ledere (LiSICON) forbindelser.
Sist, men ikke minst, har systematiske undersøkelser med forskjellige aprotiske polare løsningsmidler vist at den større ioniske radiusen til Na forårsaker en svakere desolvasjonsenergi. Den mindre Li har en høyere overflateladningstetthet rundt kjernen enn Na når begge har samme valens. Li blir derfor termodynamisk stabilisert ved å dele flere elektroner med de polare løsningsmiddelmolekylene. Det vil si at Li kan klassifiseres som en type Lewis-syre. Som et resultat er det nødvendig med en relativt høy desolvasjonsenergi for den sterkt polariserte Li, noe som fører til en relativt stor overføringsmotstand som induseres av transporten av Li fra flytende tilstand (elektrolytt) til fast tilstand (elektrode). Siden desolvasjonsenergien er nært knyttet til overføringskinetikken som forekommer ved væske/faststoff-grensesnittet, er den relativt lave desolvasjonsenergien en betydelig fordel for å designe SIB-er med høy effekt.